
FYZIKA I •
FYZIKA II •
FYZIKA •
TEORETICKÁ MECHANIKA (TF1) •
KVANTOVÁ TEORIE (TF2)
STATISTICKÁ FYZIKA (TF3) •
VZTAH MATEMATIKY A FYZIKY (TF4) •
OBECNÁ RELATIVITA (TF4)
ELEKTROMAGNETICKÉ POLE (TF4) •
FYZIKA PLAZMATU •
ASTROFYZIKA •
ASTRONOMICKÝ KURZ
ELEKTŘINA A MAGNETIZMUS (MIT) •
MODULY •
STŘEDNÍ ŠKOLY
FYZIKA – TERMODYNAMIKA (PŘÍKLADY)
|
|
Raketa |
|
|
Ryba |
|
|
Barometrická formule |
|
|
Vodorovný vrh |
|
|
Měrná tepla |
|
|
Úplné a neúplné diferenciály |
|
|
Účinnost tepelného stroje |
|
|
Růst ledu na rybníce |
|
|
Reálný plyn |
Příklad 1: Raketa
Zadání: na oběžné dráze se nachází raketa o objemu 10 m3. Uvnitř je vakuum. Nějakým způsobem vpravíme dovnitř 1 cm3 (1 gram) vody. Určete tlak vodních par, který vznikne v raketě. Teplota lodi i vody je 100 K.
Předpoklady: Jde o izotop vody H2O, známe hmotnost jednoho nukleonu mp.

Řešení: Tlak spočteme ze stavové rovnice p = NkBT/V. Počet částic určíme jako podíl hmotnosti kapky a jedné molekuly vody: N = m/m0 = m/(18 mp).
Výsledek: je 4.6 Pa.
Příklad 2: Ryba
Zadání: Ryba vypustí na dně rybníka, v hloubce 5 m, bublinu (T = 10 °C, V = 1 cm3). Určete její objem na povrchu rybníka (T = 20 °C).
Předpoklady: Zanedbejte absorpci molekul plynu do vody (N = const).
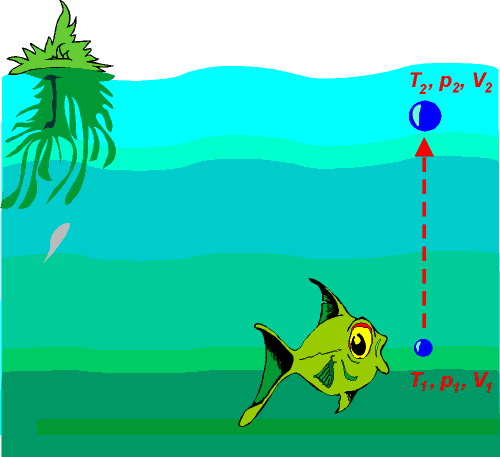
Řešení: Využijeme stavovou rovnici při konstantním počtu částic: p1V1/T1 = p2V2/T2. Odsud plyne:
V2 = (p1/p2)(T2/T1) V1.
Známé hodnoty:
p1 = patm + hρg = 1.5×105 Pa
p2 = patm = 1.0×105 Pa
T1 = 283 K
T2 = 293 K
V1 = 1 cm3
Výsledek: V2 = 1.55 cm3.
Modifikace (pro nepodprůměrné studenty): Zkuste si najít závislost velikosti bubliny na hloubce za předpokladu, že teplota roste ode dna k povrchu lineárně. Zkuste sestavit pohybovou rovnici bubliny (silou je vztlak) a řešit pohyb bubliny v závislosti na čase.
Příklad 3: Barometrická formule
Zadání: Určete rozložení tlaku s výškou nad povrchem Země.
Předpoklady: Výška atmosféry (stovky km) je vzhledem k poloměru Země malá a proto budeme předpokládat, že na jednotlivé molekuly (dusíku) působí místo celkové gravitační síly jen tíhová síla m0g, m0 je hmotnost jedné molekuly. Teplota v atmosféře je konstantní.

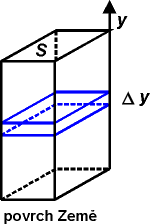
Řešení: Vrstva atmosférického sloupce tloušťky Δy zvýší povrchový tlak o Δp = ΔF/ S = − m0g ΔN / S, kde ΔN je počet částic ve vrstvě, který určíme ze stavové rovnice p ΔV = ΔN kBT. Objem ΔV = S Δy. Je-li vrstva limitně tenká, získáme diferenciální rovnici
dp / dy = − (m0g /kBT ) p .
Diferenciální rovnici vyřešíme standardními metodami pro řešení lineárních diferenciálních rovnic prvního řádu. Můžeme sestavit charakteristickou rovnici nebo rovnici řešit metodou separace.
Výsledek: Barometrická formule
p(y) = p(0) exp[− m0gy / kBT ].
Příklad 4: Vodorovný vrh
Zadání: Nalezněte mechanickou práci vykonanou tíhovým polem při vodorovném vrhu (po různých trajektoriích). Je diferenciální forma pro mechanickou práci ve tvaru úplného diferenciálu?
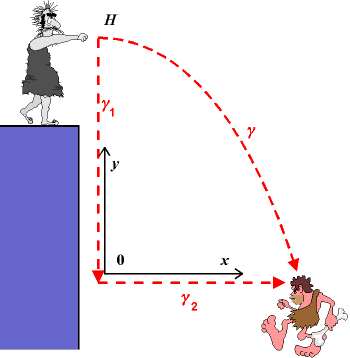
Řešení:
Silové pole: F = (0 , − mg )
Parametrické zadání křivek a jejich diferenciálů je (parametr t nemusí mít vždy význam času):
γ: (x = v0t, y = H − gt2/2); t ∈ <0, (2H/g)1/2>,
γ1: (x = 0, y = t); t ∈ <H, 0>,
γ2: (x = t, y = 0); t ∈ <0, xd> ,
dγ: (dx = v0 dt, dy = − gt dt),
dγ1: (dx = 0, dy = dt),
dγ2: (dx = dt, dy = 0),
Koncový čas u křivky γ jsme určili z podmínky dopadu y = 0. U křivek γ1 a γ2 má t význam parametru křivky a neodpovídá času jako u křivky γ. Vykonaná práce je
ΔA = ∫γ F·dx = ∫γ (Fx·dx + Fy·dy) = ∫γ (0·dx − mg·dy).
Snadno zjistíme, že je splněna podmínka ∂Fx/∂y = ∂Fy/∂x, a proto je diferenciální forma ve tvaru totálního diferenciálu a výsledek tedy nemůže záviset na integrační cestě:
Výsledek:
ΔA = ∫γ (Fx·dx + Fy·dy) = ∫0√(2H/g)(0·0 + mg·gt dt) = mgH,
ΔA = ∫γ1+γ2(Fx·dx + Fy·dy) = ∫H0(0·0 − mg dt) + ∫0xd(0·dt − mg 0) = mgH.
Příklad 5: Měrná tepla
Zadání: Určete měrná molární tepla Cp a Cv pro jednoatomární plyn. Určete měrná tepla cp a cv za normálních podmínek, je-li hustota plynu 1.3 kg m−3.
Předpoklady: Za normální podmínky považujeme atmosférický tlak
pA = 105 Pa a pokojovou teplotu T = 300 K.

Řešení: Vyjdeme z Mayerova vztahu CP = CV + R a z Poissonova vztahu CP/CV = (f+2)/f. Oba vztahy chápeme jako soustavu rovnic pro neznámá molární tepla. Po vyřešení máme:
CV = (f /2)R,
CP = (f /2 + 1) R .
Nyní zbývá určit měrná tepla cP a cV. Z definic tepel C, c
C ≡ (∂Q/∂T)/n,
c ≡ (∂Q/∂T)/m.
plyne vztah c = n/m C. Počet molů n určíme ze stavové rovnice pV = nRT a hmotnost plynu z definice hustoty ρ = m/V. Dostaneme tak
cV = CV p/(ρRT),
cP = CP p/(ρRT).
Výsledek: CV = 12.45 JK−1mol−1, CP = 20.75 JK−1mol−1, cV = 385 JK−1kg−1, cP = 641 JK−1kg−1.
Příklad 6: Úplné a neúplné diferenciály
Zadání: 1 m3 plynu za normálních podmínek je zahřán nejprve isochoricky na teplotu 600 K a poté isobaricky na teplotu 1800 K. Určete celkovou vykonanou práci, změnu tepelné energie, vnitřní energie a entropie. Určete tyto změny, došlo-li by k přechodu do koncového stavu přímo po přímce v pV diagramu. Porovnejte výsledky s tím, co víte o úplných a neúplných diferenciálech. Jakou mechanickou práci by plyn vykonal, kdyby byl děj kruhový?
Předpoklady: Plyn je dvojatomární. Za normální podmínky
považujeme atmosférický tlak pA = 1
atm = 105 Pa a pokojovou teplotu T = 300 K.
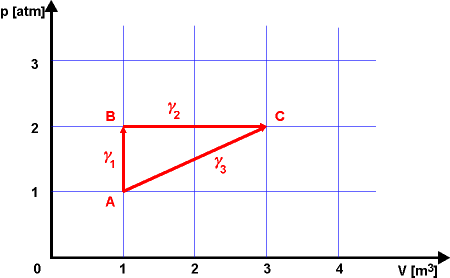
Řešení: Ze stavové rovnice pV = NkBT, respektive pV = nRT určíme stavové parametry jednotlivých bodů:
| A: | TA= 300 K | pA= 1 atm | VA= 1 m3 |
| B: | TB = 600 K | pB = 2 atm | VB = 1 m3 |
| C: | TC = 1800 K | pC = 2 atm | VC = 3 m3 |
Navíc pro všechny tři body je ve stavové rovnici shodný výraz α = nR = NkB = pV/T = 1/300 atm m3 K−1, který souvisí s množstvím plynu.
Snadno určíme rovnice všech tří křivek (γ3 je úsečka procházející body A a C):
γ1: V = VA,
γ2: p = pB,
γ3: p(V) = pA + (pC − pA) (V− VA)/(VC − VA).
Nejprve spočtěme vykonanou mechanickou práci po obou cestách:
ΔA1 + ΔA2 = ∫γ1p dV + ∫γ2p dV = 0 + pB (VC − VB) = 4 atm m3 = 4×105 J,
ΔA3= ∫γ3pdV = ∫VAVC[pA + (pC − pA) (V− VA)/(VC − VA)] dV = 3 atm m3 = 3×105 J.
Povšimněte si, že hodnoty odpovídají přesně ploše pod příslušnými křivkami. Práce není úplný diferenciál a proto po různých cestách vyšel různý výsledek. Po uzavřené křivce je integrál mechanické práce nenulový a geometricky má význam plochy uzavřené křivkou v pV diagramu:
∮γ1+γ2−γ3p dV = ΔA1 + ΔA2 − ΔA3 = (0 + 4 − 3)×105 J = 1×105 J.
Určeme nyní například integrál entropie. Obecně platí:
dS = nCV dT/T + nR dV/V = α [(f/2) dT/T + dV/V].
Po jednotlivých cestách máme:
ΔS1 = ∫γ1dS = α[(f/2) ln 2],
ΔS2 = ∫γ2dS = α[(f/2) ln 3 + ln 3] = α[(f/2) + 1] ln 3,
ΔS3 = ∫γ3dS = α[(f/2) ln 6 + ln 3] = α[(f/2) ln 2] + α[(f/2) + 1] ln 3.
Je vidět, že ΔS1 + ΔS2 = ΔS3. Integrál po obou cestách je stejný, protože entropie je úplným diferenciálem. Po uzavřené křivce je integrál entropie nulový (Clausiova rovnice), tj.
∮γ1+γ2−γ3dS = ΔS1 + ΔS2 − ΔS3 = 0.
Podobně bychom postupovali při určování dalších veličin (vnitřní energie, která je úplným diferenciálem a tepelné energie, která není úplným diferenciálem).
Příklad 7: Účinnost tepelného stroje
Zadání: Určete maximální možnou účinnost tepelného stroje, který je chlazený proudící vodou (T = 20° C) a ohříván vodní párou (T = 200° C).

Řešení: Využijeme Carnotův vztah η = (T − T0)/T. Podle Carnotovy věty jde o největší možnou účinnost. Pozor! Hodnoty je třeba zadat v absolutní teplotní stupnici.
Výsledek: 38 %.
Příklad 8: Růst ledu na rybníce
Zadání: Určete funkci času, podle které narůstá led na hladině rybníka. Zjistěte za jakou dobu naroste deseticentimetrová vrstva při teplotě −5 °C.
Předpoklady: Led přirůstá na spodní straně (na styku ledu s vodou), kde je teplota rovna teplotě fázového přechodu, tj 0 °C. Měrné skupenské teplo tání l, koeficient tepelné vodivosti λ, hustotu ledu ρ a jiné potřebné hodnoty naleznete v tabulkách materiálových konstant.
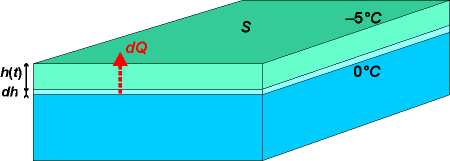
Řešení:
Ve vrstvě, kde se mění voda v led se uvolňuje tepelná energie dQ = l dm = l ρ dV = l ρ S dh. Toto teplo musí být odvedeno skrze vrstvu ledu podle vztahu: dQ/dt = λ(S·∇)T = λS ΔT/h. Porovnáním obou vztahů získáme diferenciální rovnici:
dh/dt = λΔT/(lρh),
kterou řešíme separací proměnných:
∫0hhdh = λΔT/(lρ) ∫0tdt.
Po integraci nalezneme řešení
h(t) = [2 λΔT/(lρ)]1/2 t1/2.

Výsledek: Vidíme, že led zpočátku narůstá rychle. Později se nárůst zpomaluje, protože odvod tepla probíhá tlustší vrstvou ledu. Deseticentimetrová vrstva ledu naroste při venkovní teplotě −5° C cca za dva dny.
Příklad 9: Reálný plyn
Zadání: Určete rozměry molekul reálného plynu, znáte-li jeho kritické parametry. Řešte pro vodu a CO2.
Předpoklady: Předpokládáme, že se reálný plyn chová podle van der Waalsovy rovnice (stavová rovnice opravená na vlastní objem molekul a na kohézní tlak). Potřebné hodnoty konstant naleznete v tabulkách materiálových konstant.
Řešení: Van der Waalsovu rovnici pro jeden mol plynu (p + a/V 2)(V − b) = RT přepíšeme do tvaru kubické rovnice pro objem a dosadíme kritickou teplotu a tlak:
pcV 3 − (pcb + RTc)V 2 + aV − ab = 0.
Van der Waalsova rovnice má buď tři, nebo jedno reálné řešení. Kritická izoterma je degenerovaný případ, při kterém všechna tři reálná řešení splynou. Rovnice kritické izotermy proto musí mít tvar (V − Vc)3 = 0. Po roznásobení porovnáme koeficienty obou vyjádření a získáme soustavu rovnic
pcb + RTc = 3Vc pc ,
a = 3pcVc 2,
ab = Vc 3pc .
Jde o vztah mezi kritickými parametry plynu a Van der Waalsovými konstantami a a b. Z experimentu zpravidla známe hodnoty Tc a pc. Z rovnic vyloučíme kritický objem (např. vydělíme třetí a druhou rovnici a Vc dosadíme do první a druhé rovnice) a nalezneme konstanty a a b:
a = (27/64)R2Tc 2/pc ,
b = RTc /(8pc).
Konstanta b má význam objemu jednoho molu molekul plynu. Objem jedné molekuly proto bude V0 = b/NA a lineární rozměr molekuly bude r0 ~ V01/3.
Výsledek:
Pro CO2: b = 4.26×10−5 m3 mol−1, r0 ~ 4.1×10−10 m.
Pro H2O: b = 3.05×10−5 m3 mol−1, r0 ~ 3.7×10−10 m.
| Termo | Kmity | Vlny | Elmg | Optika | Relativita | Kvanta |
| Příklady | Příklady | Příklady | Příklady | Příklady | Příklady | Příklady |
