|
| |||
|
Týdeník věnovaný aktualitám a novinkám z fyziky a astronomie. | |||
|
Nízkoteplotní plazma zastavuje krvácení
Vítězslav Kříha
Plazma generované za atmosférického tlaku je moderním nástrojem využívaným v řadě povrchových úprav. Ošetření plazmatem umožňuje například ovlivnit smáčivost, mechanické a biologické vlastnosti různých povrchů. Není divu, že se postupně začíná plazma uplatňovat jako terapeutický nástroj a v posledním desetiletí vznikla nová disciplína na pomezí fyziky a lékařství – plazmová medicína. Jednou z perspektivních oblastí rozvoje plazmové medicíny je zastavování krvácení například při klasických i endoskopických operacích. Ve své podstatě je tato technologie čtvrtým vývojovým stupněm kauterizace jako metody zastavení krvácení. Jako první stupeň byly využívány klasické kautery, kovové nástroje rozžhavené na vysoké teploty, kterými se poraněná plocha popálila. Kauterizace na druhém stupni již využívá elektrického ohřevu aktivní části nástroje a bezprostřední přenos tepla od nástroje ke tkáni. Elektrochirurgie pak přichází s nástroji, které využívají průchodu vysokofrekvenčního proudu tkání. Současné elektrochirurgické aparatury již umožňují ošetření tkáně v režimu označovaném jako fulgurace, kdy je fakticky vytvářen vysokofrekvenční výboj mezi pracovní elektrodou a tkání. Specializované aplikátory, které vytvářejí nízkoteplotní plazma za atmosférického tlaku, jsou zatím využívány spíše empiricky a na pochopení mechanizmů interakce plazmatu s tkání závisí, nakolik budou do budoucna tyto metody ještě šetrnější k ošetřovaným tkáním. V praxi se již využívají argonovéArgon – prvek patřící mezi vzácné plyny, které tvoří necelé 1 % zemské atmosféry. Jde o nereaktivní bezbarvý plyn bez chuti a zápachu. Objev argonu je oficiálně připisován lordu Rayleighovi a Williamu Ramsayovi, kteří ho detekovali roku 1894. Jako inertní atmosféra se využívá v metalurgii, při balení potravin, v plazmových technologiích i ve výbojkách. jednotky, které díky hoření výboje v argonové atmosféře chudé na kyslíkKyslík – Oxygenium, plynný chemický prvek, tvoří druhou hlavní složku zemské atmosféry. Je biogenním prvkem a jeho přítomnost je nezbytná pro existenci většiny živých organizmů na naší planetě. V atmosféře tvoří plynný kyslík 21 objemových %. Kromě obvyklých dvouatomových molekul O2 se kyslík vyskytuje i ve formě tříatomové molekuly jako ozon O3. Produkty hoření se nazývají oxidy, dříve kysličníky. Kyslík je třetím nejhojnějším prvkem ve vesmíru. snižují jednak poškození tkáně vysoce reaktivními částicemi, jednak se výrazně snižuje množství kouře, které při výkonu vzniká. To je významné jak z hlediska stavu operační optiky, tak z hlediska zdraví operatérů i pacientů.
|
Plazma – kvazineutrální soubor nabitých a neutrálních částic, který vykazuje kolektivní chování. Lidsky to znamená, že se v dané látce nachází elektricky nabité částice. Kladné a záporné náboje se navzájem kompenzují, takže celek je elektricky neutrální. Částice jsou schopné reagovat na elektrická a magnetická pole jako celek. Plazma vzniká odtržením elektronů z elektrického obalu atomárního plynu nebo ionizací molekul. S plazmatem se můžeme setkat v elektrických výbojích (blesky, jiskry, zářivky), v polárních zářích, ve hvězdách, ve slunečním větru a v mlhovinách. Pro plazma jsou typické silně nelineární jevy a nestability. Přes 99 % atomární látky ve vesmíru je v plazmatickém skupenství. Plazma (krevní) – tekutá složka krve jantarové barvy. Spolu s krvinkami tvoří krev. Pro krevní plazmu používáme ženský rod, pro plazma, jakožto ionizovaný plyn, střední rod. Plazma (minerál) – šedozeleně zbarvený chalcedon, odrůda křemene s kryptokrystalickou strukturou (je tvořen velice malými krystaly, takže se prostým okem jeví jako celistvý). Chemicky je to oxid křemičitý s příměsemi oxidů hliníku, hořčíku, vápníku, železa, chromu a niklu, které ovlivňují výsledné zabarvení, často velice pestré. Hemostáza – soubor současně probíhajících a navzájem se ovlivňujících dějů, které jsou cíleny na zastavení krvácení. Na hemostáze se podílí činnost krevních destiček, reakce poškozené cévní stěny a hemokoagulace. Hemokoagulace – srážení krve, proces vytváření třírozměrné sítě z bílkoviny fibrinu. Do této sítě se zachytávají krvinky. Proces hemokoagulace probíhá jako kaskáda enzymatických reakcí, kdy jsou na každém stupni kaskády neaktivní enzymy přeměňovány na enzymy aktivní. Enzymy spolu s dalšími látkami, které jsou schopny na jednotlivém stupni koagulační kaskády spustit přeměnu neaktivního enzymu na aktivní, jsou označovány jako koagulační faktory. Tato kaskáda je k vysvětlení významu jednotlivých koagulačních faktorů v klasickém výkladu rozdělována na vnitřní, vnější a společnou koagulační cestu. V živém organizmu probíhají vnější i vnitřní cesta společně a místo nich jsou faktory zařazovány do iniciační a amplifikační fáze. Konečným stupněm kaskády je vytvoření stavebního prvku fibrinové sítě – monomerního fibrinu z bílkoviny fibrinogenu. Monomerní fibrinogen polymerizací vytváří fibrinovou síť, zpočátku volnou, která je následnými enzymatickými reakcemi stabilizována vytvářením příčných kovalentních můstků mezi jednotlivými řetězci fibrinu za účasti vápenných kationtů. Protrombinový čas – PT, tromboplastinový čas, Quickův test. PT je doba, která popisuje schopnost krevní plazmy konkrétního jedince vytvářet vnější koagulační cestou krevní sraženinu. Aktivovaný parciální tromboplastinový čas – aPTT je doba, která popisuje schopnost krevní plazmy konkrétního jedince vytvářet vnitřní koagulační cestou krevní staženinu. Trombinový čas – TT je doba, která popisuje schopnost krevní plazmy konkrétního jedince vytvářet společnou koagulační cestou krevní staženinu. |
O plazmě a plazmatu v češtině
Slovo plazma je řeckého původu a v češtině, stejně jako i v jiných jazycích, se usadilo hned v několika vědních oborech. Plazma je tělesná tekutina, například součást krve nebo obsah buňky, mineralogie označuje slovem plazma rohovcovitý, šedozeleně zbarvený nerost a ve fyzice je plazma ionizovaný plyn vykazující kvazineutralitu a kolektivní chování či extrémní stav hmoty z volných kvarkůKvarky – částice, ze kterých jsou tvořeny těžké částice s vnitřní strukturou (hadrony). Hadrony dělíme na baryony složené ze tří kvarků (například protony a neutrony) a na mezony tvořené kvarkem a antikvarkem (například piony). Kvarky se dělí do tří generací, první tvoří kvarky „d“ (down) a „u“ (up), druhou kvarky „s“ (strange) a „c“ (charm) a třetí kvarky „b“ (bottom nebo beauty) a „t“ (top nebo truth). Kvarky mají neceločíselné (třetinové a dvoutřetinové) elektrické náboje. Jsou také nositeli barevného náboje silné interakce. a gluonůGluony – intermediální (polní, výměnné) částice silné interakce, která působí na hadrony a je krátkého dosahu. Tato interakce spojuje kvarky v mezony a baryony, udržuje pohromadě neutrony a protony v atomovém jádře a způsobuje některé rychlé rozpady elementárních částic. Celkem známe 8 gluonů. Tyto polní částice jsou nositeli barevného náboje (náboje silného interakce). Tím se silná interakce odlišuje od elektromagnetické a slabé interakce.. Termín plazma v biologii jako první použil Jan Evangelista Purkyně v první polovině devatenáctého století. Do češtiny přešlo podobně třeba drama, téma, sperma nebo klima ve svém původním středním rodu. V průběhu dvacátého století se však v biologii a mineralogii slovo plazma začalo podobně jako ve slovenštině či ruštině používat v ženském rodě. Ve fyzice bylo plazma poprvé použito Irvingem Langmuirem v roce 1927. Do češtiny tak plazma v tomto fyzikálním významu vstoupilo opět ve svém původním středním rodě, který si zatím ponechalo. Vzhledem k tomu, že s rozvojem plazmové medicíny se dá očekávat, že se častěji v jednom textu bude hovořit jak o „té“ plazmě (krevní), tak o „tom“ plazmatu (ionizovaném plynu), můžeme být za historicky vzniklé rozlišení mezi plazmou a plazmatem vděční. Historické prameny naznačují, že na rozdíl od slovenštiny či ruštiny za tuto jazykovou pestrost vděčíme citu pro jazyk fyziků plazmatu působících ve dvacátém století.
Jan Evangelista Purkyně (1787–1869); Irving Langmuir (1881–1957)
Minerál plazma nalezený v roce 2008 v Hončově Hůrce. Zdroj: Ivo Vašina.
Hemostáza
Živé organizmy se snaží udržet své vnitřní prostředí stálé i při měnících se vnějších podmínkách. Extrémní změnou ze strany vnějších podmínek je zásah do celistvosti organizmu, například poraněním. U obratlovců je výměna dýchacích plynů, živin a zplodin látkové výměny a zároveň obrana před cizorodými, tělu cizími objekty, například mikroorganizmy, zajišťována pomocí krve. Síť cév rozvádějících krev po organizmu prochází většinou tkání. Narušení celistvosti organizmu je tak zpravidla provázeno krvácením, které pro organizmus představuje ztráty jak z hlediska živin, tak, zejména v případě větších ztrát, v zajištění krevního zásobení organizmu a funkčnosti krevního oběhu. Zástava krvácení je tak jedním z důležitých mechanizmů udržení vnitřního prostředí.
Představme si pro zjednodušení krevní cévu jako hadici s vodou. Co uděláme, když se hadice poruší a začne z ní unikat voda? Máme několik možností: zastavit nebo snížit průtok vody, ucpat otvor například kolíkem, překrýt otvor záplatou, obalit hadici hadrem nebo omotat lepicí páskou, ucpat celou hadici a vést vodu od nejbližšího kohoutku či rozbočky jinými hadicemi do konečného místa, nebo nahradit poškozenou část hadice pomocí spojek kusem nové hadice. Podívejme se na jednotlivé nápady a asi nás nepřekvapí, že příroda přišla na totéž.
Zastavení či snížení tlaku vody samozřejmě omezí ztráty a usnadní případnou následnou opravu defektu v hadici. Nejrychlejší reakcí na narušení celistvosti cévy je reakce cévní stěny. Céva se stáhne díky přímému poškození hladké svaloviny v cévní stěně, uvolněním látek obsažených v buňkách vystýlajících cévy a také jako reakce na bolestivý podnět. Je to ale řešení pouze provizorní, které napomáhá ostatním mechanizmům. Krevní zásobení není možné dlouhodobě omezit.
Ucpání otvoru zátkou je provizorní řešení, které je účinné jen v případě malých defektů. Zatímco u hadice umisťujeme obvykle zátku z vnějšku, organizmus si rychle vytvoří zátku k ošetření drobných defektů v cévní stěně pomocí zátky vzniklé splynutím krevních destiček, které jsou součástí krve. Jakkoli se nám může ucpávání hadic kolíkem zdát odbytým řešením, z hlediska organizmu je třeba mít na zřeteli poměrně malou nákladnost tohoto řešení jak z hlediska časového, tak z hlediska živin. Pro správné pochopení významu tohoto řešení si musíme uvědomit, že k drobným poškozením cév vlastně dochází průběžně i při zcela běžných činnostech.
Překrytí otvoru záplatou se hodí pro větší defekty, kdy už se zátka v otvoru neudrží. Snížení ztrát ze stříkání či vytékání na pouhé prosakování je sice provizorní, ale ztráty může významně omezit. Vyřazení dané větve rozvodu z provozu je řešením v případě, kdy má síť více alternativních cest k zásobení téže cílové oblasti. Tyto tři mechanizmy se v přírodě realizují hemokoagulacíHemokoagulace – srážení krve, proces vytváření třírozměrné sítě z bílkoviny fibrinu. Do této sítě se zachytávají krvinky. Proces hemokoagulace probíhá jako kaskáda enzymatických reakcí, kdy jsou na každém stupni kaskády neaktivní enzymy přeměňovány na enzymy aktivní. Enzymy spolu s dalšími látkami, které jsou schopny na jednotlivém stupni koagulační kaskády spustit přeměnu neaktivního enzymu na aktivní, jsou označovány jako koagulační faktory. Tato kaskáda je k vysvětlení významu jednotlivých koagulačních faktorů v klasickém výkladu rozdělována na vnitřní, vnější a společnou koagulační cestu. V živém organizmu probíhají vnější i vnitřní cesta společně a místo nich jsou faktory zařazovány do iniciační a amplifikační fáze. Konečným stupněm kaskády je vytvoření stavebního prvku fibrinové sítě – monomerního fibrinu z bílkoviny fibrinogenu. Monomerní fibrinogen polymerizací vytváří fibrinovou síť, zpočátku volnou, která je následnými enzymatickými reakcemi stabilizována vytvářením příčných kovalentních můstků mezi jednotlivými řetězci fibrinu za účasti vápenných kationtů., vytvořením prostorové sítě z bílkoviny fibrinu. Fibrinová síť může vytvořit záplatu, do které se mohou zachytit krvinky, fibrin působí jako tkáňové lepidlo, které slepí oddělené kousky tkání v okolí poškozených cév, fibrinová zátka může i zcela uzavřít průsvit zcela poškozené cévy. Na úrovni kapilár, které tvoří síť s řadou spojek, je toto řešení zcela přirozené. Hemokoagulace probíhá za vhodných podmínek, například při stlačení rány během několika minut a jejím výsledkem je strup.
Výměna hadice za novou v přírodě probíhá průběžně, jak zátka ze splynulých krevních destiček, tak fibrinová zátka slouží jako vodící struktury pro růst buněk ze zdravého okolí, které nakonec obnoví funkčnost poškozené tkáně. Jakkoli může hadice omotaná netěsnící lepicí páskou vzbuzovat úsměv, jednotné řešení, kdy o zástavu krvácení se stará krev sama, budí pokornou úctu svou univerzálností, kdy tentýž mechanizmus hemokoagulace zajišťuje zamezení ztrát na několika obranných úrovních a zároveň již připravuje definitivní opravu defektu.
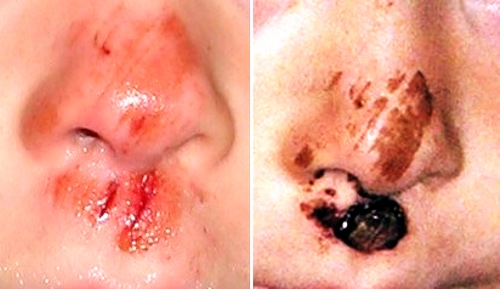
Hemostáza u oděrky s drobnými tržnými rankami. Obličej patří k dobře prokrveným částem těla, takže i drobné rány dramaticky krvácí. Vlevo: Poranění na nose jsou mělká a k zastavení krvácení na většině zasažené plochy stačilo pouze stažení kapilár a reakce destiček. Uniklá krev byla setřena při stavění krvácení a rána je pokrytá pouze prosáklou plazmou bez červených krvinek. Hlubší tržné ranky jsou zachyceny ve stádiu stabilizované fibrinové sítě, ve které jsou zachyceny červené krvinky. U pravé ranky je viditelné, že stabilizace fibrinové sítě je provázena smrštěním fibrinové zátky. Při tomto smrštění bylo vytlačeno krevní sérum, patrné jako jantarově zbarvená kapička pod rankou. Vpravo: Hojení po šesti dnech. Oděrky na nose jsou překryty strupy vzniklými koagulací prosáklé plazmy s malým množstvím zachycených červených krvinek. Na dolním rtu prvotní fibrinová zátka nestačila k fixaci tržných zranění a ranky začaly znovu krvácet. Strup z většího koagula ponechaného po druhotném krvácení nejen překryl defekty, ale i díky působícímu mechanickému napětí (vzniklému při stabilizaci fibrinové sítě) zabránil opětovnému krvácení po větších pohybech rtu při jídle a mluvení.
Hemokoagulace
Řešení zástavy krvácení i vytvoření vodící struktury pro obnovení poškozené tkáně přeměnou látek obsažených přímo v krvi je z jedné strany velice výhodné, protože poškození tkáně je zpravidla provázeno krvácením, takže jsou potřebné suroviny okamžitě dostupné. Z druhé strany nás musí okamžitě vyděsit, co se stane, když se tvorba sítě z fibrinových vláken spustí, aniž by k poškození tkáně skutečně došlo. V krevním řečišti by se pak vytvořily sraženiny, které by mohly ucpat drobné cévy v mozku, míše, srdci, plicích, ledvinách, játrech, střevě, oku…
A co hůř, potřebné bílkoviny se vytváří v játrech a potřebují na to určitý čas. Pokud by se bílkoviny na neúčelné srážení krve spotřebovaly na místech, kde jich nejen není třeba, ale i škodí, budou pak chybět v případě, kdy je krvácení třeba zastavovat. Tento děsivý scénář nazývaný diseminovaná intravaskulární koagulopatie, se naštěstí uskutečňuje pouze ve vzácných případech. U zdravého organizmu tomuto život ohrožujícímu stavu zabraňuje uspořádání mechanizmů hemokoagulace do složité kaskády, která je ovlivňována řadou látek označovaných jako koagulační faktory. Většina faktorů je označována římskými číslicemi I-XIV. Tyto faktory jsou většinou v krvi v neaktivní formě. EnzymatickouEnzymy – jednoduché či složené bílkoviny, které katalyzují chemické přeměny v živých organizmech. reakcí se přeměňují na aktivovaný koagulační faktor, označovaný písmenem „a“ u číslice faktoru, například Xa. Faktory I, Ia, II a IIa jsou pro svůj význam označovány klasickými názvy fibrinogen, fibrin, protrombin a trombin. Aktivace koagulačních faktorů je zpravidla katalyzována jiným aktivovaným koagulačním faktorem. Na jednotlivých úrovních kaskády se uplatňují kladné a záporné zpětné vazby, které ovlivňují, zdali se koagulační faktor změní na aktivovaný. Jako celek je koagulace jištěna dalším mechanizmem, označovaným jako fibrinolýza, kdy bílkovina plazmin, která rovněž vzniká kaskádovým mechanizmem, může odbourávat již vytvořený fibrin.
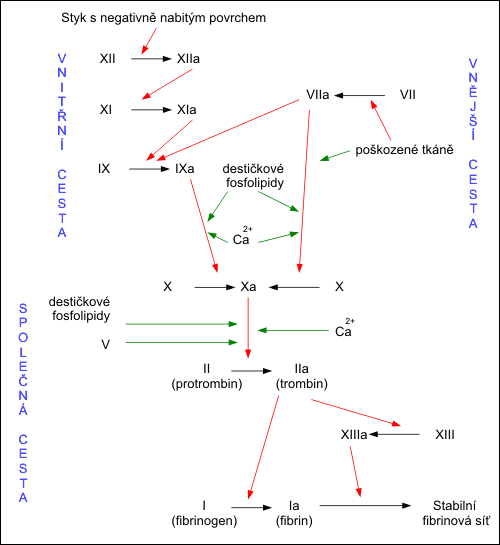
Klasický mechanizmus hemokoagulace. S mechanizmem hemokoagulace
se blíže můžete seznámit v interaktivním
Atlasu fyziologie a patofyziologie.
Protrombinový čas, aktivovaný parciální tromboplastinový čas a trombinový čas
Současný stav poznání ukázal, že v živém organizmu probíhá hemokoagulaceHemokoagulace – srážení krve, proces vytváření třírozměrné sítě z bílkoviny fibrinu. Do této sítě se zachytávají krvinky. Proces hemokoagulace probíhá jako kaskáda enzymatických reakcí, kdy jsou na každém stupni kaskády neaktivní enzymy přeměňovány na enzymy aktivní. Enzymy spolu s dalšími látkami, které jsou schopny na jednotlivém stupni koagulační kaskády spustit přeměnu neaktivního enzymu na aktivní, jsou označovány jako koagulační faktory. Tato kaskáda je k vysvětlení významu jednotlivých koagulačních faktorů v klasickém výkladu rozdělována na vnitřní, vnější a společnou koagulační cestu. V živém organizmu probíhají vnější i vnitřní cesta společně a místo nich jsou faktory zařazovány do iniciační a amplifikační fáze. Konečným stupněm kaskády je vytvoření stavebního prvku fibrinové sítě – monomerního fibrinu z bílkoviny fibrinogenu. Monomerní fibrinogen polymerizací vytváří fibrinovou síť, zpočátku volnou, která je následnými enzymatickými reakcemi stabilizována vytvářením příčných kovalentních můstků mezi jednotlivými řetězci fibrinu za účasti vápenných kationtů. podle vnitřní i vnější cesty současně a z funkčního hlediska je výhodnější na hemokoagulaci hledět z pohledu iniciace děje, amplifikační fáze a trombin-fibrinové fáze. I přesto je klasický mechanizmus hemokoagulace stále využívaný z toho důvodu, že na jeho základě vznikly standardizované diagnostické metody, které jsou široce využívány v diagnostice onemocnění krevní srážlivosti, nemocech jater, nedostatku vitamínu K, otravách jedy proti hlodavcům, případně nastavení dávky léků ovlivňujících srážlivost, zejména protisrážlivých.
Protrombinový časProtrombinový čas – PT, tromboplastinový čas, Quickův test. PT je doba, která popisuje schopnost krevní plazmy konkrétního jedince vytvářet vnější koagulační cestou krevní sraženinu. je doba, která popisuje schopnost krevní plazmy konkrétního jedince vytvářet vnější koagulační cestou krevní sraženinu. Spočívá v odebrání žilní krve, ve které se zabrání srážení přidáním roztoku citronanu sodného. Citronan na sebe naváže vápenné ionty, které jsou jedním z faktorů koagulační kaskády. Vzniklá nesrážlivá krev je promíchána, a jsou z ní odstředěním odděleny krvinky. Vzniklá krevní plazma je doplněna definovaným množstvím tromboplastinové reagencie a vápennou solí, která vyruší působení citronanu. Měří se čas od přidání reagencie do vzniku krevní sraženiny – koagula. Vznik koagula se stanovuje opticky rozptylem světla nebo mechanicky změnou odporu předmětu, který se v plazmě pohybuje díky vnějšímu magnetickému poli. Protrombinový čas je často normalizovaný poměrem s kontrolou, eventuelně ještě umocněný na korekční faktor ISI, mezinárodní index citlivosti, aby bylo možné srovnávat výsledky různých laboratoří bez ohledu na použité tromboplastinové reagencii.
Zcela analogicky se testuje vnitřní dráha koagulační kaskády pomocí aktivovaného parciálního tromboplastinového časuAktivovaný parciální tromboplastinový čas – aPTT je doba, která popisuje schopnost krevní plazmy konkrétního jedince vytvářet vnitřní koagulační cestou krevní staženinu. (aPPT). Jako reagencie se přidává aktivátor, nejčastěji kaolin a fosfolipid kefalin, označovaný jako parciální tromboplastin. Jako výsledek se opět měří doba vzniku koagula. Společná cesta hemokoagulace je testována pomocí trombinového časuTrombinový čas – TT je doba, která popisuje schopnost krevní plazmy konkrétního jedince vytvářet společnou koagulační cestou krevní staženinu., kdy se měří doba vzniku koagula přidáním ke vzorku plazmy trombinu v nadbytku, který přeměňuje fibrinogen na fibrin a tím způsobí vznik koagula.
Plazmatem na plazmu
Plazmová koagulace se vyvíjí podobně jako mnoho jiných úspěšně vyvíjených nástrojů: Lidský pokrok začal použitím klacku, nikoli zkoumáním jeho vlastností. Ošetření tkání nízkoteplotním plazmatem si již našlo své místo v chirurgických oborech, dermatologii, estetické medicíně, vnitřním lékařství, začínají hledat své místo v zubním lékařství, či onkologii. Jedním z úkolů současné fyziky plazmatu je poodhalení mechanizmů působení plazmatu na koagulaci.
Ošetření kapky krve nízkoteplotním plazmatem: Nahoře detail svítící části výboje při ošetření kapky krve, vlevo po 15 sekundách ošetření, vpravo kontrola. Kapky krve byly umístěny na povrch z nerezové oceli na jednu minutu. Zdroj: [9].
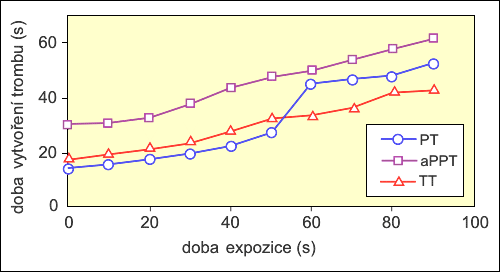
Test vnější (PT), vnitřní (aPPT) a společné (TT) dráhy koagulační kaskády v závislosti na době expozice plazmy nízkoteplotním plazmatem. Tato závislost byla překvapením, protože naznačuje, že namísto očekávaného zkrácení doby vytvoření trombu se při delších expozicích plazmy plazmatem doby koagulace prodlužují [9].
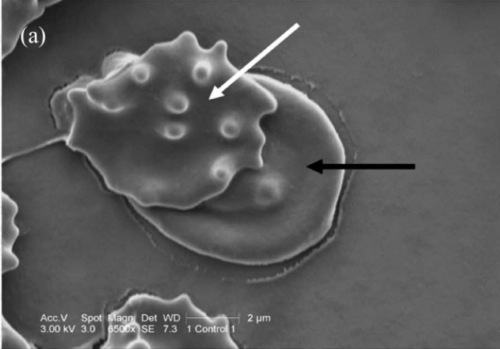
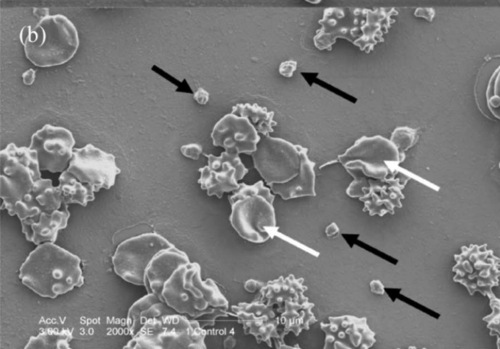
Hemostáza z pohledu rastrového elektronového mikroskopu. Pohled na kontrolu krve s přídavkem citronanu sodného. Aktivovaná krevních destička (bílá šipka) je viditelná na povrchu červené krvinky (černá šipka) [8].
Pohled na kontrolu krve s přídavkem citronanu sodného s menším zvětšením. Vedle bíle označených červených krvinek jsou na snímku zdůrazněny neaktivované krevní destičky [8].
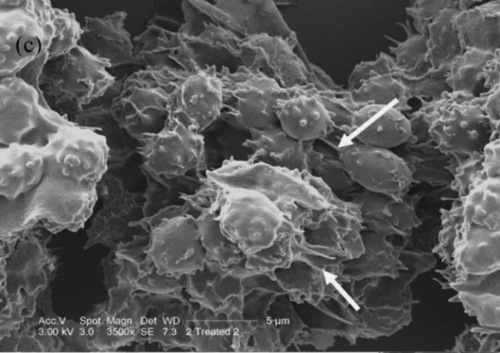
Pohled na krev s přídavkem citronanu sodného po expozici plazmatem. Je patrná četnější aktivace destiček s tvorbou panožek označených bílými šipkami. U levé hrany snímku je patrná destičková zátka vzniklá splynutím více aktivovaných destiček [8].
Pohled na krev s přídavkem citronanu sodného po expozici plazmatem. Je patrná četnější aktivace destiček s tvorbou panožek, které navzájem splývají a přispívají k vytvoření destičkové zátky. Bílými šipkami jsou zdůrazněna fibrinová vlákna vytvářející na podložce síť [8].
Je pravděpodobné, že sám o sobě poměrně složitý proces hemostázyHemostáza – soubor současně probíhajících a navzájem se ovlivňujících dějů, které jsou cíleny na zastavení krvácení. Na hemostáze se podílí činnost krevních destiček, reakce poškozené cévní stěny a hemokoagulace. se při a po působení plazmatu ještě více komplikuje, zejména z pohledu systému regulací a zpětných vazeb. Reaktivní částice vytvářené v roztoku expozicí krve plazmatem chemicky mění samotné koagulační faktory a také ovlivňují buněčnou složku krve, krvinky. Na samotnou krevní plazmu zjevně působí nízkoteplotní plazma přesně opačně, než by se z empirických zkušeností s koagulací plné krve mohlo zdát. Tato skutečnost ukazuje na provázanost regulace hemokoagulace s reakcí buněčné složky. Při pokusech ve zkumavce je po působení plazmatu patrná aktivace destiček. V živé tkáni musíme do úvah o mechanizmech koagulace plazmatem zahrnout i aktivitu cévní stěny a lokální elektrická a proudová pole.
Klip týdne: Koagulace argonovým plazmatem u zánětu tlustého střeva
Zákrok u muže (věk 76 let) po radioterapii pro karcinom prostaty. Následkem ozáření došlo ke změnám v konečníku, které vedly k epizodám, při kterých docházelo k vylití krve z konečníku po nucení na stolici či bez možnosti volně ovlivnit tento děj. Při endoskopii jsou patrná rozšíření cév ve sliznici i oblasti krvácení do sliznice. Po ošetření výbojem v argonové atmosféře jsou dobře viditelné bílé oblasti, ve kterých došlo ke koagulaci krve přímo v cévách. U výboje je patrná vláknitá struktura, typická pro výboje za atmosférického tlaku. Černá trubice na snímku je pohled na endoskop procházející konečníkem z vnitřku tlustého střeva, endoskop je ve střevě otočen o 360 stupňů a má v zorném poli sám sebe. Po šesti týdnech se krvácení snížilo o 80 %. Následovala druhá kůra, ve které byly ošetřeny zbývající rozšířené cévy. Další kontrola následovala po devíti týdnech, kdy po ošetření již mohl být pacient propuštěn z pravidelného sledování. Zdroj: Dave Project. (mp4, 37 MB)
Odkazy