|
| |||
|
Týdeník věnovaný aktualitám a novinkám z fyziky a astronomie. | |||
|
Atomy helia v extrémních magnetických polích
Miroslav Havránek
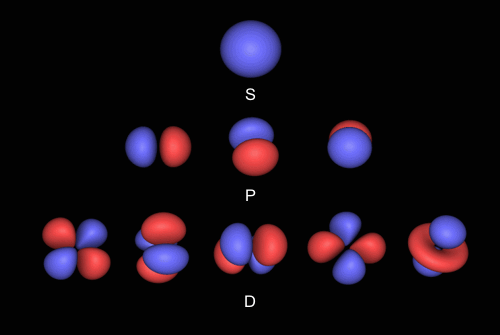
Atom heliaHelium – plynný chemický prvek, patřící mezi vzácné plyny a tvořící druhou nejvíce zastoupenou složku vesmírné hmoty. Bezbarvý plyn, bez chuti a zápachu, chemicky zcela inertní. Francouzský astronom Pierre Janssen objevil helium ze spektrální analýzy sluneční korony. V roce 1895 se britskému chemikovi Williamu Ramsayovi podařilo izolovat plynné helium na Zemi. Je pojmenované po starořeckém bohu Slunce, Héliovi. (4He) se skládá z jádra obsahujícího dva protonyProton – částice složená ze tří kvarků (duu) se spinem 1/2, hmotností 1,673×10−27 kg (938 MeV) a elektrickým nábojem +1,6×10−19 C. Proton je na běžných časových škálách stabilní, pokud se rozpadá, je poločas rozpadu větší než 1035 let. Za objevitele protonu je považován Ernest Rutherford, který v roce 1911 objevil atomové jádro při analýze rozptylu částice alfa pronikající tenkou zlatou fólií. Samotná jádra vodíku (protony) detekoval v roce 1918 při ostřelování dusíku částicemi alfa. Antiproton byl objeven v roce 1955 Emilio Segrem a Owenem Chamberlainem. a dva neutronyNeutron – částice složená ze tří kvarků (ddu) se spinem 1/2, hmotností 1,675×10−27 kg (940 MeV) a nulovým elektrickým nábojem. Volné neutrony jsou nestabilní se střední dobou života 886 s (15 minut) a poločasem rozpadu 10 minut. V roce 1930 Walther Bothe a Herbert Becke ostřelovali lehké prvky alfa částicemi a objevili nový druh pronikavého záření. V roce 1932 zjistil James Chadwick, že je toto záření složeno z neutrálních částic přibližné velikosti protonu a objevil tak neutron.. Jádro je zahaleno do elektronového obalu, který tvoří dva elektronyElektron – první objevená elementární částice. Je stabilní. Hmotnost má 9,1×10−31 kg a elektrický náboj 1,6×10−19 C. Elektron objevil sir Joseph John Thomson v roce 1897. Existenci antičástice k elektronu (pozitron) teoreticky předpověděl Paul Dirac v roce 1928 a objevil Carl Anderson v roce 1932.. Pokud atom není vystaven vnějším vlivům, tak se elektrony uspořádají do nejnižší možné energetické konfigurace, do jediného elektronového orbitaluOrbital – oblast v atomárním či molekulárním obalu, kde se vyskytuje elektron. Pravděpodobnost výskytu elektronu v orbitalu je rovna druhé mocnině velikosti komplexní vlnové funkce. (orbital S), avšak s opačnou orientací spinuSpin – vlastní (vnitřní) rotační moment částice souvisící s Lorentzovou symetrií. Pro částici v centrálním poli se přirozeným způsobem skládá s momentem hybnosti. Částice s nenulovým spinem se mohou chovat jako elementární magnetické dipóly μ, aniž by měly elektrický náboj. Takové částice reagují na vnější magnetická pole., aby byl splněn Pauliho vylučovací principPauliho vylučovací princip – „Dva fermiony nemohou být nikdy ve stejném kvantovém stavu“. Právě proto různé elektrony v atomárním obalu zaujímají různé kvantové stavy a tím vytvářejí různorodé chování chemických prvků. . Protože orbital S je plně obsazen elektrony, helium se velmi nerado účastní chemických vazeb a z chemického hlediska patří mezi inertní plyny podobně jako neonNeon – plynný chemický prvek, patřící mezi vzácné plyny. Nevytváří sloučeniny. Neon byl objeven v roce 1898 Williamem Ramsayem a Morrisem Traversem. Využívá se v osvětlovacích tělesech a světelných indikátorech. Slouží jako náplň do některých typů laserů., argonArgon – prvek patřící mezi vzácné plyny, které tvoří necelé 1 % zemské atmosféry. Jde o nereaktivní bezbarvý plyn bez chuti a zápachu. Objev argonu je oficiálně připisován lordu Rayleighovi a Williamu Ramsayovi, kteří ho detekovali roku 1894. Jako inertní atmosféra se využívá v metalurgii, při balení potravin, v plazmových technologiích i ve výbojkách. a další. Z fyzikálního hlediska lze atom helia považovat za bosonBosony – částice, které mají celočíselný spin, symetrickou vlnovou funkci, nesplňují Pauliho vylučovací princip a podléhají Boseho-Einsteinově statistickému rozdělení. Například jsou to všechny skalární i vektorové mezony, fotony a gluony. Při nízkých teplotách se bosony mohou hromadit v základním stavu. – tedy částici s celočíselným spinem. Tato vlastnost umožňuje heliu vytvořit Boseho-Einsteinův kondenzátBEC – Boseho-Einsteinův kondenzát (Bose Einstein Condensate, BEC), představuje stav hmoty, ve kterém jsou všechny částice v jednom jediném kvantovém stavu. Vlnové funkce se vzájemně překrývají a při fázovém přechodu vznikne společná vlnová funkce. Soustava částic se začne chovat jako jediná „superčástice“. Boseova-Einsteinova kondenzace vzniká u bosonů, které se mohou nacházet všechny v nejnižším energetickém stavu. Na rozdíl od běžné kondenzace, jako je tomu u fázových přechodů plynů na pevné látky, jde o kondenzaci v prostoru hybností. Přechod od klasického stavu ke kvantovému je náhlý, až dramatický. Kvantové chování se projevuje při teplotě nižší, než je tzv. teplota degenerace. za velmi nízké teploty (2,17 K).
Tvary atomových orbitalů podle rostoucího hlavního kvantového čísla. Zdroj MOE.
|
Pauliho vylučovací princip – „Dva fermiony nemohou být nikdy ve stejném kvantovém stavu“. Právě proto různé elektrony v atomárním obalu zaujímají různé kvantové stavy a tím vytvářejí různorodé chování chemických prvků. Bílý trpaslík – jedna z možných závěrečných fází vývoje hvězd. Hvězda, ve které degenerovaný elektronový plyn vyvíjí gradient tlaku (způsobený Pauliho vylučovacím principem), který odolává gravitaci. Poloměr je 1 000 km až 30 000 km, hustota řádově 103 kg cm-3, maximální hmotnost 1,4 MS. Hmotnější bílí trpaslíci jsou nestabilní, explodují jako supernovy typu Ia. Tuto tzv. Chandrasekharovu mez odvodil Subrahmanyan Chandrasekhar v roce 1930. Objev prvního bílého trpaslíka: Již v roce 1834 Fridrich Bessel předpověděl průvodce Síria A z newtonovské teorie na základě vlnovkovité trajektorie hvězdy Sírius. Tento průvodce (Sírius B) byl objeven v optické dílně bratří Clarků roku 1862 (Alvan Clark – test objektivu průměru 45 cm). Sírius B je prvním známým bílým trpaslíkem. Byla na něm demonstrována správnost newtonovské teorie (vlnovkovitá trajektorie Síria A) i potvrzena OTR (červený posuv). Sírius B je enormně malý a hustý bílý trpaslík s průměrem 11 736 km, ρ = 3×103 kg cm−3. Povrchová teplota je 24 800 K, vzdálenost 8,6 l.y. a hmotnost 1,03 MS. Neutronová hvězda – těleso tvořené degenerovaným neutronovým plynem o hmotnosti menší než přibližně 2,2 až 3 MS (Tolmanova-Oppenheimerova-Volkoffova mez). Typický průměr neutronové hvězdy je v řádu desítek kilometrů, průměrná hustota 1017 kg m−3 dosahuje hodnot hustoty atomového jádra. Neutronové hvězdy vznikají při gravitačním kolapsu velmi hmotných červených veleobrů, při výbuchu supernovy typu II. Obrovský tlak způsobuje „vtlačení“ elektronů do protonů za vzniku neutronů a neutrin. Neutronové hvězdy byly teoreticky předpovězeny ve 30. letech 20. století. Magnetar – neutronová hvězda s mimořádně silným magnetickým polem až 1012 T. Kůra je již nestabilní, praská, dochází k pravidelným magnetotřesením doprovázeným přepojením magnetických siločar a záblesky v retgenovém a měkkém gama oboru. První projevy magnetaru byly detekovány v roce 1979 (opakované záblesky gama neboli SGR). První magnetar detekovala v roce 1998 Chryssa Kouveliotou z Marshallova kosmického letového centra v NASA. Výjimečně mohou opakující se záblesky přejít v jeden mohutný, neopakovatelný záblesk. Rydbergův atom – atom excitovaný do vysokého hlavního a vedlejšího kvantového čísla. Rydbergovy atomy jsou velmi citlivé na okolní elektrická a magnetická pole. Elektronová vlnová funkce může být u některých superpozic stavů těchto atomů aproximována klasickým pohybem elektronu po kružnici. Vysoce excitované atomy jsou pojmenovány podle švédského fyzika Johannese Roberta Rydberga (1854–1919). |
Orientace spinu v magnetickém poli
Elektron je částice se spinemSpin – vlastní (vnitřní) rotační moment částice souvisící s Lorentzovou symetrií. Pro částici v centrálním poli se přirozeným způsobem skládá s momentem hybnosti. Částice s nenulovým spinem se mohou chovat jako elementární magnetické dipóly μ, aniž by měly elektrický náboj. Takové částice reagují na vnější magnetická pole. 1/2 a lze si jej představit jako elementární magnet se svým vlastním severním a jižním pólem, který se může orientovat v magnetickém poli podobně jako střelka kompasu. Energie elektronu, jehož spin míří ve směru magnetického pole, je nižší než energie elektronu orientovaného proti směru magnetického pole. V případě atomu heliaHelium – plynný chemický prvek, patřící mezi vzácné plyny a tvořící druhou nejvíce zastoupenou složku vesmírné hmoty. Bezbarvý plyn, bez chuti a zápachu, chemicky zcela inertní. Francouzský astronom Pierre Janssen objevil helium ze spektrální analýzy sluneční korony. V roce 1895 se britskému chemikovi Williamu Ramsayovi podařilo izolovat plynné helium na Zemi. Je pojmenované po starořeckém bohu Slunce, Héliovi. oba elektrony obsazují jediný orbitalOrbital – oblast v atomárním či molekulárním obalu, kde se vyskytuje elektron. Pravděpodobnost výskytu elektronu v orbitalu je rovna druhé mocnině velikosti komplexní vlnové funkce. s antiparalelně orientovanými spiny. Pokud atom vložíme do magnetického pole, spiny elektronů mají tendenci se zorientovat ve směru pole, a snížit tak svoji energii. Tato konfigurace je ale zakázána v rámci Pauliho vylučovacího principuPauliho vylučovací princip – „Dva fermiony nemohou být nikdy ve stejném kvantovém stavu“. Právě proto různé elektrony v atomárním obalu zaujímají různé kvantové stavy a tím vytvářejí různorodé chování chemických prvků. . Pokud je ale magnetické pole dostatečně silné, může jeden z elektronů přejít na vyšší energetickou hladinu (tedy do jiného kvantového stavu), a tam překlopit svůj spin a změnit tak elektronovou konfiguraci atomu helia. Toto se může ale stát pouze tehdy, pokud je energie získaná překlopením spinu vyšší, než rozdíl energie mezi těmito energetickými hladinami. Energie překlopení spinu závisí na indukci magnetického pole a výše popsaný proces se proto může odehrát pouze v prostředí o magnetické indukci 104÷105 T. Zvídavý čtenář jistě neodolá si tuto hodnotu pole vypočítat sám. Návod na řešení lze nalézt například ve třetím dílu Feynmanových přednášek z fyziky [5].
Molekuly v blízkosti neutronových hvězd
Molekuly jsou vázané stavy několika atomů, kde jsou některé elektrony sdíleny více atomy. Tyto sdílené elektrony obsazují takzvané molekulární orbitaly. Existují dva druhy molekulárních orbitalů: vazebné a antivazebné. Elektrony ve vazebných orbitalech mají energii nižší než původní orbital osamoceného atomu, a pokud je tento orbital obsazen elektronem, dochází k zesílení vazby mezi atomy. Naproti tomu antivazebný orbital má vyšší energii než orbital osamoceného atomu a přítomnost elektronu molekulu destabilizuje. V případě helia dojde v extrémním magnetickém poli kolmém na antivazebný orbital ke snížení energie orbitalu efektem orientace spinu elektronu v magnetickém poli. Elektrony ve vazebných i antivazebných molekulových orbitalech proto přispívají k soudržnosti molekuly. Tato vazba se nazývá kolmá paramagnetická vazba a umožňuje původně inertnímu heliu vytvářet dvouatomové molekuly. Zatím se ale nikomu takovou molekulu nepodařilo vytvořit ani pozorovat. V laboratorních podmínkách lze kontinuálně dosáhnout magnetického pole „pouze“ 30÷40 T. Dostatečně silná magnetická pole pro tvorbu heliových molekul se ale vyskytují ve vesmíru například v blízkosti bílých trpaslíkůBílý trpaslík – jedna z možných závěrečných fází vývoje hvězd. Hvězda, ve které degenerovaný elektronový plyn vyvíjí gradient tlaku (způsobený Pauliho vylučovacím principem), který odolává gravitaci. Poloměr je 1 000 km až 30 000 km, hustota řádově 103 kg cm-3, maximální hmotnost 1,4 MS. Hmotnější bílí trpaslíci jsou nestabilní, explodují jako supernovy typu Ia. Tuto tzv. Chandrasekharovu mez odvodil Subrahmanyan Chandrasekhar v roce 1930. Objev prvního bílého trpaslíka: Již v roce 1834 Fridrich Bessel předpověděl průvodce Síria A z newtonovské teorie na základě vlnovkovité trajektorie hvězdy Sírius. Tento průvodce (Sírius B) byl objeven v optické dílně bratří Clarků roku 1862 (Alvan Clark – test objektivu průměru 45 cm). Sírius B je prvním známým bílým trpaslíkem. Byla na něm demonstrována správnost newtonovské teorie (vlnovkovitá trajektorie Síria A) i potvrzena OTR (červený posuv). Sírius B je enormně malý a hustý bílý trpaslík s průměrem 11 736 km, ρ = 3×103 kg cm−3. Povrchová teplota je 24 800 K, vzdálenost 8,6 l.y. a hmotnost 1,03 MS. (105 T). Řádově silnějšími magnetickými poli disponují neutronové hvězdyNeutronová hvězda – těleso tvořené degenerovaným neutronovým plynem o hmotnosti menší než přibližně 2,2 až 3 MS (Tolmanova-Oppenheimerova-Volkoffova mez). Typický průměr neutronové hvězdy je v řádu desítek kilometrů, průměrná hustota 1017 kg m−3 dosahuje hodnot hustoty atomového jádra. Neutronové hvězdy vznikají při gravitačním kolapsu velmi hmotných červených veleobrů, při výbuchu supernovy typu II. Obrovský tlak způsobuje „vtlačení“ elektronů do protonů za vzniku neutronů a neutrin. Neutronové hvězdy byly teoreticky předpovězeny ve 30. letech 20. století. (108 T) a magnetaryMagnetar – neutronová hvězda s mimořádně silným magnetickým polem až 1012 T. Kůra je již nestabilní, praská, dochází k pravidelným magnetotřesením doprovázeným přepojením magnetických siločar a záblesky v retgenovém a měkkém gama oboru. První projevy magnetaru byly detekovány v roce 1979 (opakované záblesky gama neboli SGR). První magnetar detekovala v roce 1998 Chryssa Kouveliotou z Marshallova kosmického letového centra v NASA. Výjimečně mohou opakující se záblesky přejít v jeden mohutný, neopakovatelný záblesk. (1012 T).
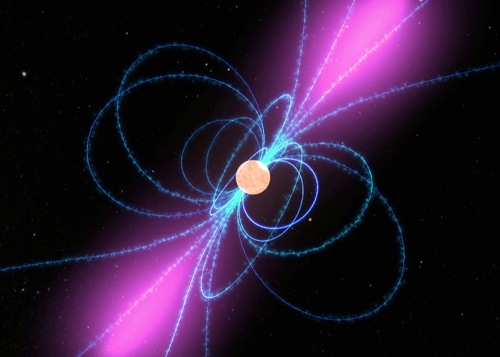
Umělecké ztvárnění pulsaruPulsar – neutronová hvězda, jejíž magnetická a rotační osa nemají shodný směr. Zářící oblasti v magnetických pólech hvězdy díky rotaci vytvářejí pro pozorovatele majákovým efektem pulzy, zpravidla radiové, výjimečně až rentgenové či gama. První pulzar byl objeven v roce 1967 Jocelyne Bellovou pod vedením Anthony Hewishe. (neutronové hvězdy). Magnetické silokřivky znázorňují dipólový charakter magnetického pole. V blízkosti magnetické osy pulsaru dochází k emisi synchrotronového záření (znázorněno fialově). Zdroj: NASA.
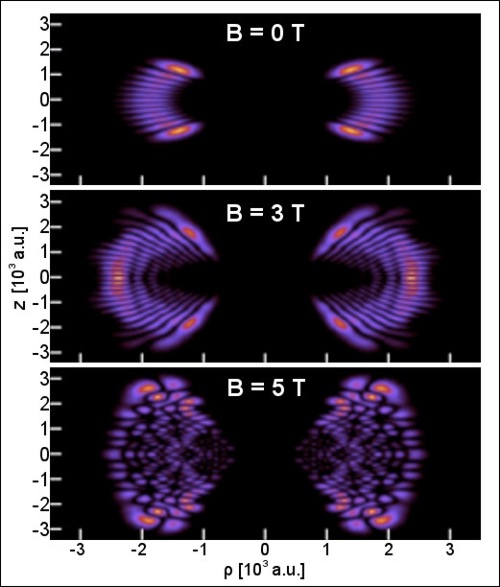
Magnetické pole na povrchu Země dosahuje hodnot pouze několika desítek μT. Vzhledem k tomu, že helium je druhým nejhojnějším prvkem ve vesmíru, tak by se heliové molekuly mohly vyskytovat například v atmosférách některých bílých trpaslíků. Experimentální důkazy o existenci těchto exotických molekul by mohly přinést výsledky přesných spektroskopických měření záření plynu okolo těchto objektů. Jinou možnost zkoumání chování atomů v extrémních magnetických polích umožňuje studium Rydbergových atomůRydbergův atom – atom excitovaný do vysokého hlavního a vedlejšího kvantového čísla. Rydbergovy atomy jsou velmi citlivé na okolní elektrická a magnetická pole. Elektronová vlnová funkce může být u některých superpozic stavů těchto atomů aproximována klasickým pohybem elektronu po kružnici. Vysoce excitované atomy jsou pojmenovány podle švédského fyzika Johannese Roberta Rydberga (1854–1919).. Právě díky velké vzdálenosti elektronů od jádra je možné tyto elektrony ovlivňovat podstatně slabším magnetickým polem, než jaké bychom potřebovali k dosažení podobných efektů v případě normálních atomů. Teoretickým studiem formování molekul v extrémních magnetických polích se zabývá norská výzkumná skupina z Univerzity v Oslo, která za tímto účelem vyvinula simulační software London. Tento program dokáže numericky vyřešit Schrödingerovu rovnici pro elektrony v molekule ve vnějším magnetickém poli s využitím metody FCI (Full Configuration Interaction), která umožňuje vypočítat vlnovou funkci elektronu rozvinutou do řady Slaterových determinantůSlaterův determinant – vyjádření antisymetrické vlnové funkce soustavy N nerozlišitelných částic. Takovou vlnovou funkci můžeme zapsat jako determinant matice, jejíž sloupce číslují polohu jednotlivých částic a řádky tvoří jednočásticové vlnové funkce první, druhé, třetí, ... až N-té částice. Determinant automaticky zaručí antisymetrii vlnové funkce.. Kvadrát amplitudy vlnové funkce pak popisuje prostorové rozložení elektronů v molekule.
Vlnová funkce elektronu Rydbergova atomu v různě silných magnetických polích. Osy znázorňují polohu v atomových jednotkáchAtomová jednotka – délková jednotka pro měření vzdáleností v atomech. Je rovna tzv. Bohrovu poloměru (průměrné vzdálenosti elektronu od jádra v základním stavu atomu vodíku). 1 a.u. = 5,29×10−11 m. (1 a.u. = 5,29×10−11 m). V silném poli je dobře patrné rozštěpení elektronových orbitalů Rydbergova atomu. Zdroj [MPI].
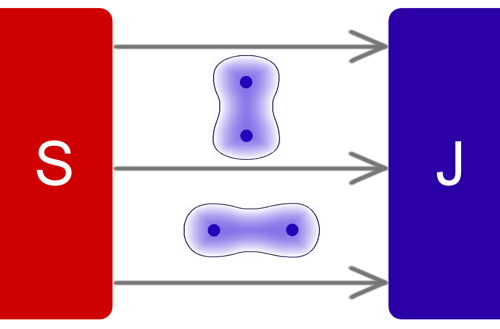
Extrémní magnetická pole mohou zesílit vazbu mezi atomy, které vytvářejí molekuly i bez magnetického pole. Příkladem jsou molekuly vodíku. Tvar a tedy i vazebná energie molekulárního orbitalu molekuly vodíku závisí nejen na velikosti magnetické indukce, ale také na směru magnetického pole. Zatímco pohyb elektronů v rovině kolmé na magnetické pole je omezen, tak se ve směru magnetických silokřivek elektrony mohou pohybovat relativně volně. Tento efekt je zodpovědný za výrazné protažení tvaru atomů a molekul ve směru magnetického pole, jak je vidět na obrázku níže. V extrémním magnetickém poli tak mohou vznikat exotické lineární molekuly obsahující čtyři nebo pět atomů vodíku.
Deformace molekulových orbitalů v magnetickém poli.
Závěr
V blízkosti závěrečných stádií hvězd se silným magnetickým polem panuje zcela jiná chemie, než na jakou jsme zvyklí. Enormní magnetická pole umožňují vytvářet exotické molekuly a možná i zcela nové materiály, jejichž soudržnost je podmíněna magnetickým polem. Přestože dosažení těchto stavů hmoty je zatím mimo dosah experimentálních možností, tak díky výpočetní technice jsme schopni alespoň částečně porozumět vlastnostem hmoty v takto extrémních podmínkách.
Odkazy
- K. Lange: A Paramagnetic Bonding Mechanism for Diatomics in Strong Magnetic Fields, Science, 2012
- P. Schmelcher: Molecule Formation in Ultrahigh Magnetic Fields, Science, 2012
- T. Wogan: New chemical bonds possible in extreme magnetic fields, Physicsworld, 2012
- A. Turbiner: Charged Hydrogenic, Helium and Helium-Hydrogenic Molecular Chains in a Strong Magnetic Field, arXiv:0909.1910v1, 2009
- R. Feynman: Feynmanovy přednášky z fyziky, Fragment, 2002
- Petr Kulhánek: Návrat planetárního modelu atomu, AB 31/2008
- David Břeň: Rydbergovy atomy simulují trojanské asteroidy, AB 12/2012